 发病机制
发病机制
发病机制:PCOS的发病机制复杂,已被公认的事实是:①高LH伴正常或低水平的FSH;②雄激素增多;③恒定的雌激素水平(E1比E2高);④胰岛素抵抗(高胰岛素血症);⑤卵巢组织形态学上有多个囊性卵泡和间质增生。
1.促性腺激素释放异常 PCOS患者的血LH升高,而FSH正常或降低,LH/FSH≥2~3,静脉注射GnRH后LH可出现过度反应,认为可能原发于下丘脑-垂体功能失调。在下丘脑中多巴胺能和阿片肽能神经对GnRH神经元的抑制作用失控,可导致LH分泌增加。但更可能是雌激素的反馈抑制异常所致。非周期性的腺外转化而来的雌激素(雌酮E1)将导致对LH分泌的正反馈和对FSH分泌的负反馈抑制。LH刺激卵泡细胞增生,产生大量雄激素,雄激素不能全部转化成雌激素,进一步增加腺外芳香化E1的生成。过多雄激素使卵泡闭锁、卵巢包膜纤维化和包膜增厚。由于缺乏月经周期中期的LH峰值,出现排卵障碍(图1)。此外,有人发现PCOS患者的卵巢也可能分泌“抑制素”,抑制FSH的分泌,影响卵泡的发育成熟,出现较多囊状卵泡,近年发现高胰岛素血症和增高的IGF也可使LH分泌增多。
2.雄激素过多 在PCOS中,几乎所有的雄激素生成均增多。而性激素结合球蛋白(SHBG)减少,游离雄激素增多,活性增强。至于过多的雄激素来源于卵巢或肾上腺众说不一。大剂量GnRH激动剂可降低促性腺激素,雄烯二酮和睾酮减少,而对来源于肾上腺的DHEAS无影响。据报道大约70%的PCOS患者为卵巢源性雄激素所致:①由于类固醇激素所需酶系功能紊乱,如芳香化酶缺乏,3β-醇甾脱氢酶不足或活性下降,P45OC17A调节异常,雌激素合成障碍,大量雄激素在外周(脂肪、肝、肾内)转换为雌酮。也有人认为卵巢发育不充分使芳香化酶的活性下降。②LH脉冲频率及振幅升高,刺激卵泡膜细胞及间质细胞增生和雄激素的生成。过多的雄激素促使卵泡闭锁,卵巢粒层细胞早期黄素化,生长停止,不能排卵,形成PCOS。
本病多发生在青春期月经初潮后,推测可能起因于性成熟前期,肾上腺功能失调,持续分泌过多雄激素。此外,在应用地塞米松前后测定卵巢和肾上腺静脉血中的各种雄激素水平,其结果支持卵巢和肾上腺是PCOS过多雄激素的共同来源,发现50%PCOS患者有肾上腺源性雄激素增多。
3.雌酮过多 PCOS妇女用孕酮等药物有撤退性子宫出血,服氯底酚胺可导致卵泡成熟排卵,月经来潮,这提示PCOS患者不但雄激素水平高,而且雌激素也增多。体内活性雌激素包括雌二醇(E
2)和雌酮(E
1),E
2主要来源于卵巢,E
1则来自卵巢、肾上腺及周围组织的转换。PCOS患者非周期性E
1明显增多,E
1/F
2比率增高(正常E
1/F
2≤1),特别是
肥胖者的脂肪多,芳香化酶活性高,外周组织转换增多,E
1水平可更高,而且来源于外周组织的E
1不受垂体促性腺激素的调节,无周期性变化。持续高水平的雌激素对下丘脑-垂体的反馈调节是不正常的。
4.细胞色素P450C17A调节失常 PCOS主要缺陷是下丘脑-垂体接受异常的反馈信号。这可能与卵巢和肾上腺本身的自分泌、旁分泌调节机制障碍有关。PCOS患者常伴17-羟孕酮(17-OHP)升高,这是由于卵泡膜细胞内或肾上腺网状带内P450C17A的调节机制失常所致。P450C17A具有17-羟化酶和17,20-链裂酶的双重活性,在△4将孕酮转换为17-OHP和雄烯二酮,在△5将孕烯醇酮衍变为17-羟孕烯醇酮和DHEA。
17-羟孕酮既是肾上腺合成皮质醇的重要前体物质.也是卵巢合成性激素特别是雄激素的重要前体。若给予PCOS患者GnRH-A或HCG(特别在用地塞米松抑制后),17-羟孕酮、雄烯二酮明显升高;而ACTH兴奋试验又能促使肾上腺的DHEA与17-OHP同时增多,提示卵巢和肾上腺网状带的P450C17A活性增高。因此,P450C17A活性调节异常是肾上腺和卵巢雄激素过量分泌的重要原因。但为什么会出现类固酮合成的调节异常尚不清楚。胰岛素/IGFs系统可刺激卵巢和肾上腺P450C17A mRNA表达及其活性。此外,CYP11A的侧链裂解酶基因编码区与产生过多雄激素有关。
5.胰岛素抵抗与高胰岛素血症 PCOS患者不论有无
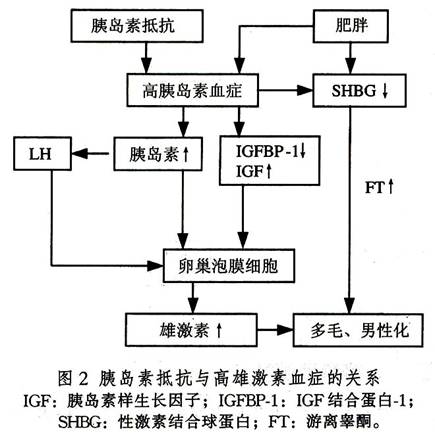
肥胖,多有不同程度的胰岛素抵抗与高胰岛素血症。近期发现大约有半数PCOS患者的发病与胰岛素受体丝氨酸磷酸化缺陷有关。因而认为胰岛素在其发病中占有重要地位。胰岛素与IGF-1通过IGF-1受体作用于卵泡膜细胞,促使雄烯二酮和睾酮合成。近年的研究发现,垂体邻近部位有胰岛素受体,或者同时存在的高IGF-1血症可促进LH刺激的卵泡膜细胞增生,导致雄激素过多和卵泡过早闭锁(图2)。Hasegawa用胰岛素增敏剂Troglitazone治疗PCOS,可使胰岛素水平降低,LH和雄激素水平相应降低也支持这一观点。胰岛素升高对调节SHBG的代谢有重要作用,可使肝脏SHBG生成减少,游离睾酮升高。此外,胰岛素受体丝氨酸磷酸化可抑制胰岛素受体活性,促进P450C17A的17,20-链裂酶活性。近年对位于染色体11pl5.5的胰岛素基因的5'-端可变数串联重复顺序(VNTR)的研究发现,胰岛素基因的VNTR是PCOS的一个主要易感位点(特别是排卵性PCOS)。说明胰岛素VNTR多态性是PCOS的遗传学因素。
6.
肥胖 PCOS伴
肥胖者(BMI≥25)占20%~60%。体脂分布不均匀。现知脂肪组织是类固醇激素的重要代谢场所,脂肪组织中的芳香化酶将外周雄激素转换为E
1和E
2。研究证实,雄烯二酮转换为E
1的量与脂肪组织总量相关,高雄激素血症时SHBG下降,游离E
2增加。雌激素使脂肪细胞生长、增殖。不同的内分泌环境能造成不同的
肥胖体态,雄激素升高表现为上身
肥胖(即男性型
肥胖),而雌激素增多者为下身
肥胖(即女性型
肥胖)。体重增加常伴血胰岛素升高和SHBG及IGFBP下降,从而使游离性激素和IGF-1增多。这类患者常伴有糖耐量异常或2型
糖尿病。
近来,Rouru等提出
肥胖-瘦素-NPY轴可能是部分PCOS患者下丘脑-垂体-LH过度分泌的病因,即
肥胖妇女的瘦素分泌增多,后者抑制下丘脑NPYmRNA表达和NPY的分泌,解除NPY对LH的抑制,促使LH大量释放。
7.高泌乳素血症 高泌乳素血症与PCOS的关系尚待进一步研究。PCOS高泌乳素血症的发生率为10%~15%,但确诊为PCOS者的PRL都轻度或中度升高,更高水平的PRL多与垂体PRL瘤有关。引起高PRL的机制尚不清楚。可能是:①PRL升高与血雌酮增多有关。②下丘脑多巴胺相对不足,用多巴胺激动剂(如溴隐亭)治疗PCOS无排卵或多毛症可获得成功。高PRL血症者卵巢对外源性促性腺激素无反应。
8.PCOS与卵巢自身免疫 研究发现,某些PCOS与卵巢自身免疫有关。PCOS患者卵泡中有淋巴细胞浸润,并存在抗卵巢细胞抗体,但Rojansky等对31例PCOS患者的研究显示,抗卵巢抗体与PCOS无相关。Luborsky等用酶免分析检测24例PCOS的抗卵巢抗体,25%PCOS患者为阳性,
绝经期妇女组与育龄妇女组的阳性率分别为22%和19%,3组阳性率无差异。因此,关于PCOS是否与卵巢自身免疫有关尚无一致结论。
卵巢病理:典型的PCOS患者有双侧卵巢对称性增大,体积可达正常的2~4倍,表面皱褶消失,平滑,呈灰白色,富含血管,包膜肥厚,包膜下有多量大小不等的卵泡,最大直径可达1.5cm,囊壁薄,囊泡周围的卵泡膜细胞增生伴黄素化,包膜增厚则是长期不排卵的结果,包膜厚度与血LH水平及男性化程度呈正相关。
 临床表现
临床表现
临床表现:PCOS的临床表现主要由于各种内分泌、代谢障碍所致,并表现出高度的异质性,临床上以卵巢功能障碍为显著标志。PCOS常始于青春期。生育期以无排卵、不育和
肥胖、多毛等典型临床表现为主,到中老年则出现因长期的代谢障碍导致的
糖尿病、心血管疾病如高血压等。因此,未得到恰当处理的PCOS可影响妇女的一生。
1.月经失调 患者的初潮年龄多为正常,但常在初潮后即出现月经失调,主要表现为月经稀发、经量少或
闭经,临床上可见从月经稀发(周期逐渐延长)至
闭经的发展过程。少数患者表现为
月经过多或不规则出血。
2.不孕 PCOS患者由于持续的无排卵状态,导致不孕。异常的激素环境可影响卵子的质量、子宫内膜的容受性、甚至胚胎的早期发育,即使妊娠也易发生流产。
3.多毛、痤疮 在高雄激素的影响下,PCOS女性呈现不同程度的多毛,发生率为17%~18%。多毛以性毛(阴毛和腋毛)浓密为主,尤其是阴毛,分布呈男性型,甚至下延及肛周,上及腹股沟或腹中线。毛发也可分布于面部口周、乳周、下颌、大腿根部等处。多毛的程度与血中雄激素升高并不平行,白种病人更为常见。极少数病例有男性化征象如声音低沉、喉结突出。过多的雄激素转化为活性更强的双氢睾酮后,刺激皮脂腺分泌过盛,可出现痤疮。
4.
肥胖 PCOS患者中40%~60%的体重指数(BMI)≥25。可能是由于雄激素过多或长期的雌激素刺激,或其他内分泌、代谢紊乱和遗传特征,引起脂肪的堆积,不但腹壁,而且腹腔内脏器官间也出现脂肪堆积,后者的危害更大,更易导致代谢异常、心血管疾病等远期合并症。
肥胖的发生与PCOS的发生发展存在相互促进的作用,
肥胖患者的胰岛素抵抗及高胰岛素血症促进PCOS的发展。
5.
黑棘皮症 PCOS患者可出现局部皮肤或大或小的天鹅绒样、片状、角化过度、呈灰棕色的病变,常分布在颈后、腋下、外阴、腹股沟等皮肤皱褶处,称
黑棘皮症,与高雄激素和胰岛素抵抗及高胰岛素血症有关。
 实验室检查
实验室检查
实验室检查:
1.LH/FSH 血LH与FSH比值与浓度均异常,呈非周期性分泌,大多数患者LH增高,而FSH相当于早期卵泡期水平,LH/FSH≥2.5~3。不少学者认为LH/FSH比例增加是PCOS的特征。
2.雄性类固醇 雄激素过多,
睾酮、
雄烯二酮、DHEA、DHEAS水平均可增高。
3.雌性类固醇 雌酮与
雌激素异常,恒定的
雌激素水平,E
2水平波动小,无正常的月经周期性变化,E
1水平增加,E
1/E
2>1。
4.PRL PCOS时可轻度升高,但因高泌乳素血症可出现类PCOS症状,应加以鉴别。
5.尿17-OHCS和17-KS 24h尿17-酮升高反映肾上腺雄激素分泌的增多。
6.地塞米松抑制试验 可抑制肾上腺性激素的分泌,服用地塞米松0.5mg,每6小时1次,共4天,服后取血样,如血清硫酸脱氢异雄酮或
尿17-酮类固醇被抑制至正常水平,可排除肾上腺肿瘤或增生之可能。
7.绒毛膜促性腺激素(HCG)刺激试验 HCG可刺激卵巢合成雄激素,注射HCG可引起血浆雄激素水平升高。
8.促皮质素(ACTH)兴奋试验 ACTH兴奋试验可促肾上腺源性雄激素DHEA及尿17-KS增高。
通过HCG刺激试验、地塞米松抑制试验、ACTH兴奋试验可帮助鉴别雄激素升高的来源。
9.阴道脱落细胞成熟指数 是初步了解体内性激素状况的简易方法。
睾酮过多的涂片往往出现3层细胞同时存在的片型,明显增高时3层细胞数几乎相等,但必须与炎症相区别。
雌激素水平可以从表层细胞百分比来估计,但不能反映血液中激素的含量。
10.基础体温测定 判断有无排卵,排卵者呈双相型,无排卵者一般为单相型。
 诊断
诊断
诊断:
1.临床诊断 初潮后多年月经仍不规则、月经稀少和(或)
闭经,同时伴
肥胖与多毛、婚后不孕等,应疑诊PCOS。典型病例具有上述各种症状及体征,即月经失调、多毛、痤疮、
肥胖、不孕等。非典型病例可表现为:①单纯性
闭经不伴有
肥胖、多毛及卵巢肿大,排除其他各种疾病,而孕酮试验阳性者,仍应考虑为PCOS。②排卵型功能失调性出血。③月经异常合并多毛。④月经异常伴男性化症状,无明显
肥胖。⑤功能失调性子宫出血伴不育。
对于不典型病例需详细询问有关病史,如起病年龄、生长发育情况,起病经过,用药史,家族史,个人生活习惯,既往有无全身性疾病。结合辅助检查,排除其他疾病,并经B超等检查明确诊断。
2.诊断标准 由于本病的异质性,诊断标准尚未统一,多数学者根据青春期发病、月经和排卵异常、多毛、血LH和(或)LH/FSH比值升高,结合一种雄激素水平过高,超声检查有多囊卵巢征象,排除其他类似疾病后,可确定本症的诊断。
日本妇产科学会生殖内分泌委员会于1993年提出PCOS诊断标准如下:
(1)临床症状:①月经异常(
闭经、月经稀发、无排卵月经等);②男性化(多毛、粉刺、声音低调、阴蒂肥大);③
肥胖;④不孕。
(2)内分泌检查所见:①LH高值、FSH正常值;②注射GnRH后LH分泌增多,FSH分泌正常;③雌酮/雌二醇比值升高;④血中睾酮或雄烯二酮升高。
(3)卵巢所见:①B超见多个卵泡囊性变;②双合诊及B超见卵巢肿大;③腹腔镜见卵巢内膜肥厚及表面隆起;④镜下见卵泡膜细胞层肥厚增殖和间质增生。
以上的(1)、(2)、(3)项是必有的项目,3项均具备时可诊断为PCOS,其他项目做为参考,若所有必备和参考项目均具备,则为典型PCOS病例。
 鉴别诊断
鉴别诊断
鉴别诊断:
1.卵巢的多囊样改变 一些青春期或生育期有排卵功能的妇女的卵巢也可以表现出类似PCOS患者卵巢的多囊样改变,临床超声显像下多见,不一定是一种病理情况。此种卵巢体积不一定增大、小卵泡数目也不如PCOS的卵巢、可见成熟卵泡,临床上缺乏PCOS的表现,各项检查指标没有PCOS的改变。
2.卵泡膜细胞增殖症 临床表现及内分泌检查与PCOS的相仿,但更为严重。特征性的病理变化是在卵巢间质中见黄素化的卵泡膜样细胞群,皮质下并无类似PCOS的许多小卵泡。其雄激素水平比一般的PCOS患者更高,男性化表现更明显,主要为卵巢来源的雄激素。硫酸脱氢表雄酮正常,LH/FSH可正常。促排卵治疗很难显效。两者临床较难鉴别,常需卵巢组织活检确诊。
3.卵巢雄激素肿瘤 极少数的
卵巢肿瘤可分泌大量雄激素,如睾丸母细胞瘤、门细胞瘤或癌等。肿瘤一般是单侧、实性,逐渐增大。患者男性化的征象更为明显,可表现为进行性。超声显像、CT或MRI有助诊断。
4.肾上腺皮质增生或肿瘤 患者肾上腺分泌大量皮质醇和雄激素,有
肥胖、多毛、月经紊乱等表现,超声检查见卵巢呈多囊性变化,但患者有肾上腺皮质功能紊乱的临床表现,肾上腺皮质增生者尿17-酮、17羟明显增高,对ACTH兴奋试验反应亢进,地塞米松抑制试验抑制率≤0.70,肾上腺皮质肿瘤患者则对这两项试验反应均不明显。
 治疗
治疗
治疗:PCOS以下丘脑垂体-卵巢轴凋节紊乱为主要表现,其发病与糖脂代谢紊乱等密切相关。多因素相互作用的病理性恶性循环,使其病变发生发展,形成从青春期起始的、持续存在的卵泡发育成熟障碍。必须多途径打破异常作用的恶性循环环节。
1.降低LH水平
(1)用短效避孕药或Diane-35(含炔雌醇0.035mg及酯酸环丙孕酮2mg)等,周期性服用,通过反馈作用降低LH的高频高幅异常分泌,使卵巢源性雄激素减少。同时,酯酸环丙孕酮可有效地对抗雄激素,抑制内源性雄激素与受体结合及5α还原酶的活性,抑制毛囊雄激素受体生成而减少毛发生长。其他的避孕药有妈富隆,其含炔雌醇30µg和地索高诺酮150µg,后者雄激素活性低,极少有增加体重的副作用。因周期性子宫内膜剥脱起到预防子宫内膜癌的作用。
(2)促性腺激素释放激素类似物(GnRHa):GnRHa可降调节垂体Gn分泌,下调细胞膜GnRH受体,使垂体LH分泌明显减少,抑制卵巢源性的雄激素分泌。常用剂型有GnRHa缓释剂:
诺雷德(zoladex 3.6mg),
达必佳(decapeptyl 3.75mg),
达菲林(dafelin 3.75mg)。于月经的第2天皮下注射,连续抑制作用达29天,最多可连续使用3个周期以避免长期的低雌激素效应,可用于要求生育而难于控制的高LH水平的PCOS患者。
2.改善PCOS的胰岛素抵抗状态 提高胰岛素靶细胞的敏感性,降低血胰岛素的水平,控制糖代谢紊乱,改善PCOS的胰岛素抵抗状态。对于肥胖的PCOS患者,以糖脂代谢紊乱为主,特别是有糖尿病家族史及糖耐量异常者,降低胰岛素尤为重要。
(1)降低体重:应强调体育锻炼,控制饮食,必要时辅予降低代谢的减肥药物。
(2)
甲福明(metformin):是双胍类,剂量为1000~1500mg/d。是治疗非胰岛素依赖型糖尿病的药物,通过降低血胰岛素,纠正PCOS患者的高雄激素血症,改善卵巢排卵功能,提高促排卵治疗的效果。
(3)二氮嗪(dizoxide):用于直接降低胰岛素的药物,300mg/d,对降低胰岛素及血游离雄激素有明确效果。
(4)噻唑烷二酮类(Thiazolidinediones,TZDs,格列酮类):主要包括
罗格列酮和
吡格列酮,是新一代的胰岛素增敏剂。它可增加靶组织对胰岛素的敏感性,直接影响受体后胰岛素信号传导和级联反应,最终改善胰岛素抵抗和高胰岛素血症;通过调节脂代谢,纠正血脂异常。格列酮类除纠正糖代谢信号途径异常外,同时是卵巢细胞分裂信号途径的抑制剂,在卵巢内发挥双重作用。TZDs为B类药物,动物实验中可导致生育能力下降,引起胚胎死亡和生长受限。因此,妊娠、哺乳妇女不宜服用本药。
3.降低雄激素水平及其受体活性 上述降LH药物及调节胰岛素分泌的药物,均可降低血雄激素水平。螺内酯(spirono1actone)是醛固酮竞争抑制剂,能与二氧
睾酮竞争靶组织的雄激素受体,也能降低17α-羟化酶活性,降低血中
睾酮水平,剂量为40~200mg/d。
4.促排卵 有生育要求者,在用GnRH-a或避孕药降低血LH或
睾酮后,使用氯米芬(clomiphene)50~150mg/d,连用5~7天,用基础体温及超声监测排卵,适时给予人绒毛膜促性腺激素(HCG)1万U肌注促排卵。若使用氯米芬无效时,可采用促性腺激素类药物如重组人促卵泡成熟激素(gonal-F)促排卵,低剂量递增。生育期不要求生育的妇女,若年龄≤38岁,仍应在调整内分泌紊乱、降LH和雄激素水平后行常规促排卵治疗,如氯米芬、他莫昔芬,保证有周期性月经来潮。若促排卵无效时,可考虑单纯黄体酮撤退性出血治疗,以预防子宫内膜癌。
5.有各种代谢紊乱的患者要注意进行相应处理,并预防和监测远期并发症的发生。
6.手术治疗 诱发排卵的药物出现前,卵巢楔形切除术一度曾是不排卵多囊卵巢综合征的惟一治疗方法。目前逐渐被各种腹腔镜下的电灼术、多点穿刺术或激光打孔术所取代。在腹腔镜下,适当固定卵巢,用单极电凝针垂直于卵巢表面或以激光瞄准卵巢表面,调整功率和工作时间,根据卵巢的大小,在卵巢表面作直径2~4mm、穿透皮质3~5mm的孔4~20个。术中注意避免损伤卵巢门附近结构和卵巢系膜的血管,影响卵巢的血液供应。适当采用防粘连措施。术后50%~90%的病人恢复排卵,妊娠率为40%甚至70%。手术治疗更适合于那些有高LH水平的患者,而对于肥胖、胰岛素抵抗的PCOS并不推荐作为优先考虑的措施。
手术治疗后可发生卵巢和盆腔粘连,也有导致卵巢早衰的个例报道。手术方法应该在药物治疗无效的情况下考虑。
手术的疗效可能与下述因素有关:减少已增大的卵巢体积、减少了异常激素如雄激素及抑制素的分泌、增加对促性腺激素的敏感性、创伤诱发生长因子的释放从而放大了FSH的作用或者破坏了旧的囊泡,使新的卵泡生长。



 流行病学
流行病学
 病因
病因
 发病机制
发病机制

 临床表现
临床表现
 并发症
并发症
 实验室检查
实验室检查
 其他辅助检查
其他辅助检查
 诊断
诊断
 鉴别诊断
鉴别诊断
 治疗
治疗
 预后
预后
 预防
预防